Auteur : Douglas Theobald, Ph.D.
Copyright © 1999-2012 - Version 2.89
Permission is granted to copy and print these pages in total for non-profit personal, educational, research, or critical purposes.
La page originale disponible à l’adresse http://www.talkorigins.org/faqs/comdesc/section1.html
Navigation :
Partie 1: L'arbre phylogénétique universel unique
Charles Darwin
The Origin of Species, p. 171
Prédiction 1.1: L'unité fondamentale de la vie
– Carolus Linnaeus
au début du Systema Naturae, 1757
Selon la théorie de la descendance commune, les organismes vivants modernes, avec toutes leurs différences incroyables, sont la progéniture d'une seule espèce dans un passé lointain. En dépit de la grande diversité de formes et de fonctions entre les organismes, plusieurs critères fondamentaux caractérisent toute vie. Certaines des propriétés macroscopiques qui caractérisent l'ensemble de la vie sont (1) la réplication, (2) l'héritabilité (les caractéristiques des descendants sont corrélées à celles des ancêtres), (3) la catalyse et (4) l'utilisation de l'énergie (métabolisme). Au minimum, ces quatre fonctions sont nécessaires pour générer un processus historique physique pouvant être décrit par un arbre phylogénétique.
Si toutes les espèces vivantes descendent d'une espèce originale qui avait ces quatre fonctions obligatoires, toutes les espèces vivantes d'aujourd'hui devraient nécessairement avoir ces fonctions (conclusion quelque peu triviale). Mais surtout, toutes les espèces modernes devraient avoir hérité des structures qui remplissent ces fonctions. Ainsi, une prédiction de base de la parenté généalogique de toute vie, associée à la contrainte du gradualisme, est que les organismes devraient être très similaires dans les mécanismes et les structures particulières qui exécutent ces quatre processus de la vie de base.
Confirmation
Les polymères communs de la vie
Les structures que tous les organismes connus utilisent pour exécuter ces quatre processus de base sont toutes assez similaires, malgré les probabilités. Tous les êtres vivants connus utilisent des polymères pour remplir ces quatre fonctions de base. Les chimistes organiques ont synthétisé des centaines de polymères différents, mais les seuls utilisés par la vie, quelles que soient les espèces, sont les polynucléotides, les polypeptides et les polysaccharides. Quelle que soit l'espèce, l'ADN, l'ARN et les protéines utilisés dans les systèmes vivants connus ont tous la même chiralité, même s'il existe au moins deux choix chimiquement équivalents de chiralité pour chacune de ces molécules. Par exemple, l'ARN possède quatre centres chiraux dans son cycle ribose, ce qui signifie qu'il existe 16 stéréoisomères possibles, mais un seul de ces stéréoisomères se trouve dans l'ARN d'organismes vivants connus.
Les acides nucléiques sont le matériel génétique de la vie
Dix ans après la publication de L'origine des espèces, les acides nucléiques ont été isolés pour la première fois par Friedrich Miescher en 1869. Il a fallu encore 75 ans après cette découverte pour que l'ADN soit identifié comme le matériel génétique de la vie (Avery et al. 1944). Il est tout à fait concevable que nous ayons pu trouver un matériel génétique différent pour chaque espèce. En fait, il est encore possible que des espèces nouvellement identifiées aient un matériel génétique inconnu. Cependant, tous les formes de vie connuss utilisent le même polymère, le polynucléotide (ADN ou ARN), pour stocker des informations spécifiques à leur espèce. Tous les organismes connus basent la réplication sur la duplication de cette molécule. L'ADN utilisé par les organismes vivants est synthétisé en utilisant seulement quatre nucléosides (désoxyadénosine, désoxythymidine, désoxycytidine et désoxyguanosine) sur des dizaines connus (au moins 102 se produisent naturellement et beaucoup d'autres ont été synthétisés artificiellement) (Rozenski et al. 1999; Voet et Voet 1995, page 969).
Catalyse des protéines Afin de remplir les fonctions nécessaires à la vie, les organismes doivent catalyser des réactions chimiques. Dans tous les organismes connus, la catalyse enzymatique est basée sur les capacités fournies par les molécules de protéines (et dans des cas relativement rares, mais importants, par les molécules d'ARN). Il existe plus de 390 acides aminés d'origine naturelle connus (Voet et Voet 1995, p. 69; Garavelli et al. 2001); cependant, les molécules de protéines utilisées par tous les organismes vivants connus sont construites avec le même sous-ensemble de 22 acides aminés.
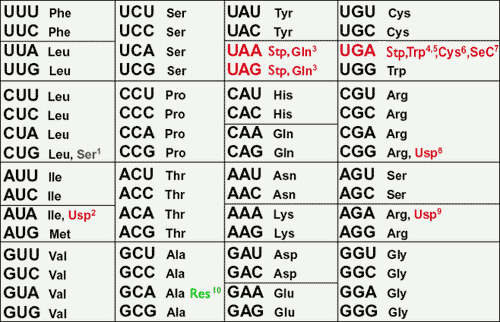
Le code génétique universel Il doit exister un mécanisme de transmission des informations du matériel génétique au matériel catalytique. Tous les organismes connus, à de très rares exceptions près, utilisent le même code génétique à cet effet. Les quelques exceptions connues sont néanmoins des variantes simples et mineures du code génétique “universel” (voir Figure 1.1.1) (Lehman 2001; Voet et Voet 1995, p. 967), exactement comme prédit par les biologistes de l'évolution à partir de la théorie de descendance commune, des années avant la résolution définitive du code génétique (Brenner, 1957; Crick et al., 1961; Hinegardner et Engelberg, 1963; Judson, 1996, p. 280-281).
Les scientifiques qui ont déchiffré le code génétique dans les années 1950 et 1960 ont travaillé en partant du principe que le code était universel ou presque (Judson 1996, p. 280-281). Ces scientifiques (parmi lesquels Francis Crick, Sydney Brenner, George Gamow et plusieurs autres) ont tous formulé cette hypothèse et l'ont justifiée en se fondant sur un raisonnement évolutif, même en l'absence de toute preuve expérimentale directe d'un code universel.
Figure 1.1.1. Le code génétique standard et les codes nucléaires variantes connus.
“Crick a demandé à ses compagnons deux autres hypothèses simplificatrices d'une grande audace. (…) ils ont supposé, avec quelque appréhension, que le code génétique serait le même pour tous les êtres vivants. Il n'y avait aucune preuve de cela; … Pourtant l’universalité semblait inévitable pour une raison évidente: puisqu’une mutation qui changerait un seul mot ou une seule lettre du code modifierait la plupart des protéines d’une créature, elle semblait à coup sûr mortelle. ” (Judson 1996, p. 280-281)
En fait, l'hypothèse d'un code génétique universel a été déterminante pour leur succès dans la résolution du code. Par exemple, en 1957, près de dix ans avant que le code génétique ne soit définitivement résolu, Sydney Brenner publia un article influent dans lequel il concluait que tous les codes de triplets qui se chevauchaient étaient impossibles si le code était universel (Brenner, 1957). Ce document a été largement considéré comme un travail de référence, car de nombreux chercheurs se tournaient vers un code à chevauchement. Bien sûr, il s'est avéré que Brenner avait raison sur la vraie nature du code.
En 1961, cinq ans avant le déchiffrement du code, Crick faisait référence au travail de Brenner dans son rapport historique dans la revue Nature, “Nature générale du code génétique des protéines” (Crick et al. 1961). Bien que l’organisme utilisé dans le document soit la bactérie E. coli, Crick a intitulé le document “le code génétique des protéines” et non “un code génétique” ou “le code génétique de E. coli”. Dans cet article, Crick et d’autres ont conclu que le code était (1) un code de triplet, (2) ne se chevauchant pas et (3) que le code est lu à partir d’un point de départ fixe (c’est-à-dire le codon “start”) (Crick et al., 1961). Ces conclusions reposaient explicitement sur l’hypothèse que le code était essentiellement identique pour le tabac, les humains et les bactéries, bien qu’il n’y ait pas de support empirique direct pour cette hypothèse. Ces conclusions, lorsqu'elles ont été appliquées à divers organismes, des bactéries aux humains, se sont révélées correctes. Ainsi, les travaux expérimentaux ont également supposé un code universel dû à une descendance commune.
En fait, en 1963, trois ans avant la résolution définitive du code, Hinegardner et Engelberg publièrent dans Science un article expliquant de manière formelle la raison pour laquelle le code devait être universel (ou presque) si la descendance commune universelle était vraie, car sinon la plupart des mutations dans le code serait probablement mortelles pour tous les êtres vivants. Notez que, bien que ces premiers chercheurs aient prédit un code génétique universel basé sur une ascendance commune, ils ont également prédit que des variations mineures pourraient probablement être trouvées. Hinegardner et Engelberg ont permis certaines variations dans le code génétique et ont prédit la distribution de cette variation si elle était trouvée:
“… si différents codes existent, ils doivent être associés à des groupes taxonomiques majeurs tels que les phylums ou les règnes qui ont leurs racines dans le passé.” (Hinegardner et Engelberg 1963)
De même, avant de trouver des codes alternatifs, Francis Crick et Leslie Orgel ont exprimé leur surprise que des variantes mineures du code n'aient pas encore été observées:
“Il est un peu surprenant que des organismes avec des codes quelque peu différents ne coexistent pas.” (Crick and Orgel 1973, p. 344)
Crick et Orgel ont eu raison de leur surprise, et nous connaissons aujourd'hui une douzaine de variantes mineures du code génétique universel standard (voir les codons gris, rouge et vert de la figure 1.1.1). Comme Hinegardner et Engelberg l'avaient prédit, les variations mineures du code génétique standard sont effectivement associées à des groupes taxonomiques majeurs (vertébrés, plantes, ciliés unicellulaires, etc.).
Métabolisme commun Tous les organismes connus utilisent des voies métaboliques et des enzymes métaboliques extrêmement similaires, sinon identiques, dans le traitement des molécules contenant de l'énergie. Par exemple, les systèmes métaboliques fondamentaux dans les organismes vivants sont la glycolyse, le cycle de l'acide citrique et la phosphorylation oxydative. Chez tous les eucaryotes et chez la majorité des procaryotes, la glycolyse est effectuée à travers les mêmes dix étapes, dans le même ordre, en utilisant les mêmes dix enzymes (Voet et Voet, 1995, p. 445). De plus, l'unité la plus élémentaire de stockage de l'énergie, la molécule d'adénosine triphosphate (ATP), est la même chez toutes les espèces étudiées.
Réfutation potentielle
Des milliers de nouvelles espèces sont découvertes chaque année, et de nouvelles séquences d'ADN et de protéines sont déterminées chaque jour à partir d'espèces auparavant non examinées (Wilson 1992, Ch. 8). Au rythme actuel, qui augmente de façon exponentielle, près de 30 000 nouvelles séquences sont déposées chaque jour auprès de GenBank, soit plus de 38 millions de nouvelles bases séquencées chaque jour. Chacun est un test de la théorie de la descendance commune. Quand j'ai écrit ces mots pour la première fois en 1999, le taux était inférieur au dixième de ce qu'il est aujourd'hui (en 2006), et nous avons maintenant 20 fois la quantité d'ADN séquencée.
Sur la seule base de la théorie de la descendance commune et de la génétique d'organismes connus, nous prédisons fortement que nous ne trouverons jamais d'espèces modernes provenant de phylums connus sur cette Terre possédant un matériel génétique étranger, sans acide nucléique. Nous faisons également la forte prévision que toutes les espèces nouvellement découvertes appartenant aux phyla connus utiliseront le “code génétique standard” ou un dérivé proche de celui-ci. Par exemple, selon la théorie, aucun des milliers d'insectes nouveaux et inconnus qui sont constamment découverts dans la forêt tropicale brésilienne n'aura de génome sans acide nucléique. Ces espèces d'insectes, encore non découvertes, n'auront pas non plus de codes génétiques qui ne soient pas des dérivés proches du code génétique standard. En l'absence de la théorie de la descendance commune, il serait fort possible que chaque espèce ait un code génétique très différent, spécifique, puisqu'il existe 1,4 x 10^70 codes génétiques informationnellement équivalents, tous utilisant les mêmes codons et acides aminés comme code génétique standard (Yockey 1992). Cette possibilité pourrait être extrêmement utile pour les organismes, car elle exclurait les infections virales interspécifiques. Cependant, cela n'a pas été observé et la théorie de la descendance commune interdit effectivement une telle observation.
Autre exemple, neuf nouvelles espèces de lémuriens et deux espèces de marmouset (tous des primates) ont été découvertes dans les forêts de Madagascar et du Brésil en 2000 (Groves 2000; Rasoloarison et al. 2000; Thalmann et Geissmann 2000). Dix nouvelles espèces de singes ont été découvertes au seul Brésil depuis 1990 (Van Roosmalen et al. 2000). Rien en biologie n'empêche ces différentes espèces d'avoir un matériel génétique jusqu'alors inconnu ou un code génétique jamais utilisé auparavant - rien, sauf la théorie de la descendance commune. Cependant, nous savons maintenant définitivement que les nouveaux lémuriens utilisent l'ADN avec le code génétique standard (Yoder et al. 2000); les marmouset doivent encore être testés.
De plus, chaque espèce pourrait utiliser un polymère différent pour la catalyse. Les polymères utilisés pourraient toujours être chimiquement identiques tout en ayant des chiralités différentes selon les espèces. Il existe des milliers de voies de glycolyse thermodynamiquement équivalentes (même en utilisant les mêmes dix étapes de réaction mais dans des ordres différents), il est donc possible que chaque espèce ait sa propre voie de glycolyse, adaptée à ses propres besoins. Le même raisonnement s’applique aux autres voies métaboliques essentielles, telles que le cycle de l’acide citrique et la phosphorylation oxydative.
Enfin, de nombreuses molécules autres que l'ATP pourraient tout aussi bien servir de support de l'énergie chez différentes espèces (CTP, TTP, UTP, ITP ou toute molécule de type ATP avec l'un des 293 acides aminés connus ou l'une des dizaines d'autres bases pouvant remplacer l’adénosine). La découverte de nouveaux animaux ou de nouvelles plantes contenant l'un des exemples anormaux présentés ci-dessus constituerait une falsification potentielle d'ascendance commune, mais ils n'ont pas été retrouvés.
Prédiction 1.2: Une hiérarchie imbriquée d'espèces
Comme le montre la phylogénie de la figure 1, le modèle d'organismes prédit, sera, à un moment donné, décrit comme des “groupes dans des groupes”, également appelé hiérarchie imbriquée. Les seuls processus connus qui génèrent spécifiquement des modèles hiérarchiques uniques, imbriqués, sont des processus évolutifs à branches. La descendance commune est un processus génétique dans lequel l'état de la génération / de l'individu actuel dépend uniquement des modifications génétiques survenues depuis la plus récente population (ou individu) ancestral. Par conséquent, l'évolution progressive d'ancêtres communs doit se conformer aux mathématiques des processus de Markov et des chaînes de Markov. En utilisant les mathématiques markoviennes, il peut être rigoureusement prouvé que les systèmes de réplication markoviens à branches créent des hiérarchies imbriquées (Givnish et Sytsma 1997; Harris 1989; Norris 1997). Pour ces raisons, les biologistes utilisent régulièrement des chaînes de Markov à ramifications pour modéliser efficacement les processus évolutifs, y compris les processus génétiques complexes, les distributions temporelles des noms de famille dans les populations (Galton et Watson 1874) et le comportement épidémique des agents pathogènes.
L'organisation hiérarchique imbriquée des espèces contraste fortement avec d'autres schémas biologiques possibles, tels que le continuum de “la grande chaîne de l'être” et les continuums prédits par la théorie de la progression organique de Lamarck (Darwin 1872, p. 552-553; Futuyma 1998, p. 88-92). Une simple similitude entre les organismes ne suffit pas à supporter la macroévolution; le modèle de classification imbriqué produit par un processus évolutif de ramification, tel que la descendance commune, est beaucoup plus spécifique que la simple similitude. Les exemples du monde réel qui ne peuvent pas être classés objectivement dans les hiérarchies imbriquées sont les particules élémentaires (décrites par la chromodynamique quantique), les éléments (dont l'organisation est décrite par la mécanique quantique et illustrée par le tableau périodique), les planètes de notre système solaire, des livres dans une bibliothèque, ou des objets spécialement conçus comme des bâtiments, des meubles, des voitures, etc. Bien qu'il soit trivial de classer n'importe quoi subjectivement de manière hiérarchique, seules certaines choses peuvent être classées objectivement dans une hiérarchie imbriquée cohérente et unique. La différence établie ici entre “subjectif” et “objectif” est cruciale et nécessite quelques précisions illustré par l’exemple. Différents modèles de voitures pourraient certainement être classés hiérarchiquement - peut-être pourrait-on classer les voitures d'abord par couleur, puis dans chaque couleur en fonction du nombre de roues, puis dans chaque numéro de roue par constructeur, etc. , Toutefois, quelqu’un d’autre classeraient les voitures par taille, puis par année, puis par couleur, etc. Le système de classification choisi pour les voitures est subjectif. En revanche, les langues humaines, qui ont des ancêtres communs et qui dérivent par descendance avec modification, peuvent généralement être classées dans des hiérarchies imbriquées objectives (Pei 1949; Ringe 1999). Personne ne pourrait raisonnablement prétendre que l'espagnol devrait être catégorisé avec l'allemand plutôt qu'avec le portugais.
La différence entre la classification des voitures et la classification des langues réside dans le fait que, dans les voitures, certains caractères (par exemple, couleur ou fabricant) doivent être considérés comme plus importants que d'autres caractères pour que la classification fonctionne. Les types de caractères de voiture les plus importants dépendent des préférences personnelles de l'individu qui effectue le classement. En d'autres termes, certains types de caractères doivent être pondérés subjectivement afin de classer les voitures dans des hiérarchies imbriquées; les voitures ne tombent pas dans des hiérarchies imbriquées naturelles, uniques et objectives.
En raison de ces faits, une analyse cladistique des voitures ne produira pas d'arborescence unique, cohérente et bien soutenuee qui affiche des hiérarchies imbriquées. Une analyse cladistique de voitures (ou une analyse cladistique d’organismes imaginaires avec des caractères attribués de manière aléatoire) aboutira bien sûr à une phylogénie, mais il y aura un très grand nombre d’autres phylogénies, dont beaucoup avec des topologies très différentes, qui seront également soutenues par les mêmes données. En revanche, une analyse cladistique d’organismes ou de langues aboutira généralement à une hiérarchie imbriquée bien étayée, sans pondération arbitraire de certains caractères (Ringe, 1999). L'analyse cladistique d'un véritable processus généalogique produit un ou relativement peu d'arbres phylogénétiques bien mieux supportés par les données que les autres arbres possibles.
Il est intéressant de noter que Linné, qui a découvert à l'origine la classification hiérarchique objective des organismes vivants, a également tenté de classer les roches et les minéraux de manière hiérarchique. Cependant, sa classification pour les objets non vivants a finalement échoué, car elle a été jugée très subjective. Les classifications hiérarchiques des objets inanimés ne fonctionnent pas car, contrairement aux organismes, les roches et les minéraux n'évoluent pas par filiation avec des modifications d'ancêtres communs.
Le degré auquel une phylogénie donnée affiche un unique hiérarchie imbriquée objective et bien étayée peut être rigoureusement quantifiée. Plusieurs tests statistiques différents ont été développés pour déterminer si une phylogénie a une hiérarchie imbriquée subjective ou objective ou si une hiérarchie imbriquée donnée aurait pu être générée par un processus aléatoire plutôt que par un processus généalogique (Swofford 1996, p. 504). Ces tests mesurent le degré de “structure hiérarchique cladistique” (également connu sous le nom de “signal phylogénétique”) dans une phylogénie, et les phylogénie basées sur de véritables processus généalogiques donnent des valeurs élevées de structure hiérarchique, alors que les phylogénies subjectives qui n'ont qu'une structure hiérarchique apparente (comme une phylogénie des voitures, par exemple) donnent de faibles valeurs (Archie 1989; Faith et Cranston 1991; Farris 1989; Felsenstein 1985; Hillis 1991; Hillis et Huelsenbeck 1992; Huelsenbeck et al. 2001; Klassen et al. 1991).
Il y a une mise en garde à prendre en compte avec cette prédiction: si les taux d'évolution sont rapides, les informations cladistiques peuvent être perdues au fil du temps car elles seraient essentiellement randomisées. Plus le taux est rapide, moins il faut de temps pour effacer les informations sur le modèle historique à branche de l'évolution. Les caractères évoluant lentement nous ont laissé voir plus loin dans le temps; les caractères évoluant plus rapidement limitent cette vue aux événements les plus récents. Si le taux d'évolution d'un caractère donné est extrêmement lent, une hiérarchie imbriquée ne sera observée pour ce caractère que pour des taxons éloignésles uns des autres. Toutefois, le “taux d'évolution” par rapport au “temps écoulé depuis la divergence” est relatif; si la descente commune est vraie, alors, dans un laps de temps donné, nous pourrons toujours observer une hiérarchie imbriquée pour un caractère donné. De plus, nous savons empiriquement que différents caractères évoluent à des vitesses différentes (par exemple, certains gènes ont des taux de mutation plus élevés que d’autres). Ainsi, si la descendance commune est vraie, nous devrions observer des hiérarchies imbriquées sur une large plage de temps à différents niveaux biologiques.
Par conséquent, étant donné que la descendance commune est un processus généalogique, elle devrait produire des organismes pouvant être organisés en hiérarchies objectives imbriquées. De manière équivalente, nous prédisons qu'en général, les analyses cladistiques d’organismes devraient produire des phylogénie ayant des valeurs importantes et statistiquement significatives de structure hiérarchique (dans la pratique scientifique classique, un résultat de “grande signification statistique” est un résultat ayant une probabilité de 1% ou moins d’être attribuable au hasard [P <0,01]). En tant que représentation de la descendance commune universelle, l'arbre de vie universel devrait avoir une structure hiérarchique et un signal phylogénétique hautement significatif.
Confirmation
La plupart des espèces existantes peuvent être organisées assez facilement dans une classification hiérarchique imbriquée. Ceci est évident dans l'utilisation du schéma de classification linnéen. Sur la base de caractères dérivés partagés, des organismes étroitement apparentés peuvent être placés dans un groupe (tel qu'un genre), plusieurs genres peuvent être regroupés dans une même famille, plusieurs familles peuvent être regroupées dans un ordre, etc.
En tant qu'exemple spécifique (voir Figure 1), les plantes peuvent être classées comme vasculaires et non vasculaires (c'est-à-dire qu'elles ont ou ne possèdent pas de xylème et de phloème). Niché au sein du groupe vasculaire, il existe deux divisions, les plantes à graines et les plantes sans graines. Deux autres groupes, les angiospermes (qui ont des graines incluses et protégées) et les gymnospermes (ayant des graines non-fermées), sont nichés dans les plantes à graines. Les monocotylédones et les dicotylédones font partie du groupe des angiospermes.
Plus important encore, l'arbre phylogénétique standard et presque toutes les phylogénies évolutionnaires plus ciblées présentent des valeurs de structure hiérarchique statistiquement significatives (Baldauf et al. 2000; Brown et al. 2001; Hillis 1991; Hillis et Huelsenbeck 1992; Klassen et al. 1991). .
Réfutation potentielle
Il serait très problématique que de nombreuses espèces combinent les caractéristiques de différents groupes imbriqués. En reprenant l'exemple précédent, certaines plantes non vasculaires pourraient avoir des graines ou des fleurs, comme les plantes vasculaires, mais ce n'est pas le cas. Des gymnospermes (par exemple, des conifères ou des pins) pourraient parfois être trouvés avec des fleurs, mais ils ne le sont jamais. On peut trouver des plantes sans graines, comme des fougères, avec des tiges ligneuses; Cependant, seuls certains angiospermes ont des tiges ligneuses. On peut imaginer que certains oiseaux pourraient avoir des glandes mammaires ou des poils; certains mammifères pourraient avoir des plumes (ils sont un excellent moyen d'isolation). Certains poissons ou amphibiens pourraient avoir des dents différenciées ou en pointe, mais ce ne sont que des caractéristiques des mammifères. Un tel mélange de caractères rendrait extrêmement difficile l'organisation objective des espèces dans des hiérarchies imbriquées. Contrairement aux organismes, les voitures ont un mélange de caractères et c’est précisément pourquoi une hiérarchie imbriquée ne découle pas naturellement de la classification des voitures.
S'il était impossible, ou très problématique, de placer des espèces dans un schéma de classification objectif imbriqué (comme c'est le cas pour les exemples voiture, chaise, livre, élément atomique et particule élémentaire mentionnés ci-dessus), la macroévolution serait effectivement réfutée. Plus précisément, si l’arbre phylogénétique de toute vie donnait des valeurs de signal phylogénétique statistiquementbasses (structure hiérarchique), la descendance commune serait résolument réfutée. En fait, il est possible d’avoir un motif “réciproque” à partir de hiérarchies imbriquées. Mathématiquement, une hiérarchie imbriquée est le résultat de corrélations spécifiques entre certains caractères d'organismes. Lorsque les vitesses évolutives sont rapides, les caractères se répartissent aléatoirement les uns par rapport aux autres et les corrélations s’affaiblissent. Cependant, les caractères peuvent également être anticorrélés - il est possible qu'ils soient corrélés dans le sens contraire de ce qui produit des hiérarchies imbriquées (Archie 1989; Faith et Cranston 1991; Hillis 1991; Hillis et Huelsenbeck 1992; Klassen et al. 1991). L'observation d'un tel schéma anti-corrélé constituerait une forte réfutation de la descendance commune, quels que soient les taux d'évolution.
L'indice de cohérence (CI - consistency index ) est une mesure couramment utilisée de la structure hiérarchique cladistique. Les propriétés statistiques de la mesure de l'CE ont été étudiées dans un article, fréquemment cité, de Klassen et al. (Klassen et al. 1991; voir la figure 1.2.1). La valeur exacte de l'CI dépend du nombre de taxons dans l'arbre phylogénétique considéré. Dans cet article, les auteurs ont calculé quelles valeurs de CI étaient statistiquement significatives pour différents nombres de taxons. Des valeurs plus élevées de CI indiquent un degré plus élevé de structure hiérarchique.
Par exemple, un CI de 0,2 est attendu à partir de données aléatoires pour 20 taxons. Une valeur de 0,3 est toutefois hautement significative sur le plan statistique. Le point le plus intéressant pour le moment est le fait qu’un IC de 0,1 pour 20 taxons est également très significatif sur le plan statistique, mais trop bas - il est révélateur d’une structure anticladistique. Klassen et al. ont pris 75 valeurs de CI provenant de cladogrammes publiés en 1989 (combinées de trois articles) et ont indiqué comment elles se comportaient en termes de signification statistique. Les cladogrammes utilisaient de 5 à 49 taxons différents (c’est-à-dire des espèces différentes). Trois des 75 cladogrammes se situaient dans les limites de confiance de 95% pour les données aléatoires, ce qui signifie qu'il était impossible de les distinguer des données aléatoires. Tous les autres ont présenté des valeurs hautement significatives sur le plan statistique de l'IC. Aucun n'a montré des valeurs significativement basses; aucune ne présentait un modèle anti-corrélé, anti-hiérarchique.
Figure 1.2.1. Un graphique des valeurs de CI des cladogrammes versus le nombre de taxons dans les cladogrammes.
 Les valeurs de CI sont sur l’axe des y; le nombre de taxons est sur l'axe des x. Les limites de confiance de 95% sont indiquées en turquoise clair. Tous les points situés au-dessus et à droite de la région turquoise sont des valeurs IC statistiquement significatives. De même, tous les points situés en dessous et à gauche de la région turquoise sont des valeurs faiblement significatives d’IC. (reproduit de Klassen et al. 1991, figure 6).
Les valeurs de CI sont sur l’axe des y; le nombre de taxons est sur l'axe des x. Les limites de confiance de 95% sont indiquées en turquoise clair. Tous les points situés au-dessus et à droite de la région turquoise sont des valeurs IC statistiquement significatives. De même, tous les points situés en dessous et à gauche de la région turquoise sont des valeurs faiblement significatives d’IC. (reproduit de Klassen et al. 1991, figure 6).
Notez que cette étude a été réalisée avant la mise en place de mesures statistiquement significatives permettant aux chercheurs de “supprimer” les mauvais cladogrammes. Comme on pouvait s'y attendre, les trois “mauvais” ensembles de données étaient considérés avec moins de dix taxons - il est bien sûr plus difficile de déterminer la signification statistique avec très peu de données. Soixante-quinze études indépendantes menées par différents chercheurs, portant sur différents organismes et gènes, avec des valeurs élevées de CI (P <0,01) constituent une confirmation incroyable avec un degré astronomique de signification statistique combinée (P « 10-300, Bailey et Gribskov 1998; Fisher 1990). Si l'inverse était vrai - si de telles études donnaient des valeurs statistiques de CI (structure hiérarchique cladistique) qui étaient inférieures à celles attendues à partir de données aléatoires - la descendance commune aurait été fermement réfutée.
N'oubliez pas qu'environ 1,5 million d'espèces sont actuellement connues et que la majorité de ces espèces ont été découvertes depuis que Darwin a pour la première fois formulé son hypothèse d'ascendance commune. Et même ainsi, elles ont toutes intégrées le bon modèle hiérarchique, dans l’intervalle d’erreur de nos méthodes. De plus, on estime que seulement 1 à 10% de toutes les espèces vivantes ont été cataloguées, et encore moins étudiées en détail. De nouvelles découvertes d'espèces affluent chaque jour et chacune d'entre elles est un test de la théorie de la descendance commune (Wilson 1992, Ch. 8).
Prédiction 1.3: Rapprochement des phylogénies indépendantes
Emile Zuckerkandl et Linus Pauling, discutant de la possibilité d'une hiérarchie imbriquée jumelée avant les premières phylogénies moléculaires.
(1965) “Divergence évolutive et convergence dans les protéines.” dans Evolving Genes and Proteins, p. 101.
Ici, nous commençons à enfoncer la porte ouverte par Pauling, il y a 40 ans. S'il existe un arbre phylogénétique historique qui unit toutes les espèces dans une généalogie objective, toutes les sources de données distinctes devraient converger vers le même arbre (Penny et al. 1982; Penny et al. 1991; Zuckerkandl et Pauling 1965). Les arbres phylogénétiques de tous les organismes déterminés de manière indépendante doivent correspondre avec un degré de significativité statistique élevé.
Confirmation:
Des arbres phylogénétiques bien déterminés, déduits de preuves indépendantes de la morphologie et des séquences moléculaires, correspondent à un degré extrêmement élevé de significativité statistique. De nombreux gènes dotés de fonctions cellulaires très basiques sont omniprésents: ils se trouvent dans les génomes de la plupart ou de tous les organismes. Un exemple souvent cité est le gène du cytochrome c. Étant donné que tous les eucaryotes contiennent le gène de cette protéine essentielle, ni sa présence ni sa fonction ne sont corrélées à la morphologie de l'organisme. De plus, du fait de la redondance de codage de l'ADN, des parties de certaines séquences d'ADN n'ont absolument aucune corrélation avec le phénotype (par exemple, certains introns ou la dégénérescence de la troisième base de la plupart des codons d'ADN). En raison de ces deux aspects de certaines séquences d’ADN, à savoir l’ubiquité et la redondance, il est possible de choisir avec soin les séquences d’ADN qui constituent des données complètement indépendantes de la morphologie. (Voir les points 4.1 et 4.2 pour plus de détails sur les preuves de séquence moléculaire et sur la manière dont elles sont indépendantes de la morphologie). Le degré de congruence phylogénétique entre ces ensembles de données indépendants est tout simplement incroyable.
En science, les mesures indépendantes de valeurs théoriques ne sont jamais exactes. Lorsqu'on déduit une valeur (telle qu'une constante physique comme la charge de l'électron, la masse du proton ou la vitesse de la lumière), une erreur existe toujours dans la mesure, et toutes les mesures indépendantes sont dans une certaine mesure incongrues. Bien entendu, la science n'a jamais acquis la valeur réelle de quelque chose - nous n'avons que des mesures dont nous espérons qu'elle se rapproche de la valeur réelle. Scientifiquement, les questions pertinentes sont donc les suivantes: “Lorsqu’on compare deux mesures, quelle différence entraîne t’elle un problème?” et “A quel point les mesures doivent-elles être proches pour donner une confirmation forte?” Les scientifiques répondent à ces questions quantitativement avec des probabilités et des statistiques (Box 1978; Fisher 1990; Wadsworth 1997). Pour être rigoureux sur le plan scientifique, nous avons besoin d'une significativité statistique. Certaines mesures d'une valeur donnée correspondent à une significativité statistique (bonne), d'autres non (mauvaise), même si aucune mesure ne correspond exactement (réalité).
Dans quelle mesure les arbres phylogénétiques issus d'études morphologiques correspondent-ils aux arbres issus d'études moléculaires indépendantes? Il existe plus de 1038 façons différentes de disposer les 30 principaux taxons représentés à la figure 1 dans un arbre phylogénétique (voir tableau 1.3.1; Felsenstein 1982; Li 1997, p. 102). Malgré ces probabilités, les relations données à la figure 1, déterminées à partir de caractères morphologiques, sont complètement congruentes avec les relations déterminées indépendamment à partir des études moléculaires du cytochrome c (for consensus phylogenies from pre-molecular studies see Carter 1954, Figure 1, p. 13; Dodson 1960, Figures 43, p. 125, and Figure 50, p. 150; Osborn 1918, Figure 42, p. 161; Haeckel 1898, p. 55; Gregory 1951, Fig. page opposée au titre; pour les phylogénies de la les premières études sur le cytochrome c voir McLaughlin and Dayhoff 1973; Dickerson and Timkovich 1975, pp. 438-439). Sur le plan quantitatif, des mesures morphologiques et moléculaires indépendantes telles que celles-ci ont déterminé l’arbre phylogénétique standard, comme le montre la figure 1, avec une valeur meilleure que 38 décimales. Cette corroboration phénoménale de descendance commune universelle est appelée “hiérarchie jumelée”. Cependant, ce terme est impropre dans la mesure où il existe en réalité plusieurs hiérarchies imbriquées, déterminées indépendamment à partir de nombreuses sources de données.
Lorsque deux arbres déterminés indépendamment ne concordent pas avec certaines branches, ils sont appelés “incongrus”. En général, les arbres phylogénétiques peuvent être très incongrus et toujours correspondre à un très haut degré de significativité statistique (Hendy et al. 1984; Penny et al. 1982; Penny et Hendy 1986; Steel et Penny 1993). Même pour une phylogénie avec un petit nombre d'organismes, le nombre total d'arbres possibles est extrêmement grand. Par exemple, il y a environ mille différentes phylogénies possibles pour seulement six organismes; pour neuf organismes, il y a des millions de phylogénies possibles; pour 12 organismes, il existe près de 14 milliards de phylogénies différentes possibles (Tableau 1.3.1; Felsenstein 1982; Li 1997, p. 102). Ainsi, la probabilité de trouver deux arbres similaires par hasard via deux méthodes indépendantes est extrêmement faible dans la plupart des cas. En fait, deux arbres différents de 16 organismes dont 10 branches ne correspondent pas ont toujours une grande significativité statistique (Hendy et al. 1984, tableau 4; Steel et Penny 1993). Pour plus d'informations sur la signification statistique des arbres qui ne correspondent pas exactement, voir “Statistiques des arbres phylogénétiques incongrus”.
Figure 1.3.1. Number of possible phylogenetic trees for a given number of taxa
| Number of taxa | Number of possible trees | |
|---|---|---|
| rooted | unrooted | NR = (2n-3)!! = (2n-3)!/(2n-2(n-2)!) |
| 2 | 3 | 1 |
| 3 | 4 | 3 |
| 4 | 5 | 15 |
| 5 | 6 | 105 |
| 6 | 7 | 945 |
| 7 | 8 | 10 395 |
| 8 | 9 | 135 135 |
| 9 | 10 | 2 027 025 |
| 10 | 11 | 34 459 425 |
| 11 | 12 | 654 729 075 |
| 12 | 13 | 13 749 310 575 |
| 13 | 14 | 316 234 143 225 |
| 14 | 15 | 7 905 853 580 625 |
| 15 | 16 | 213 458 046 676 875 |
| 16 | 17 | 6 190 283 353 629 375 |
| 17 | 18 | 191 898 783 962 510 625 |
| 18 | 19 | 6 332 659 870 762 850 625 |
| 19 | 20 | 221 643 095 476 699 771 875 |
| 20 | 21 | 8 200 794 532 637 891 559 375 |
Le degré étonnant d’adéquation entre les arbres phylogénétiques même les plus incongrus que l’on trouve dans la littérature biologique est largement méconnu, principalement parce que la plupart des gens (y compris de nombreux biologistes) ignorent les mathématiques en jeu (Bryant et al. 2002; Penny et al. 1982; Penny et Hendy 1986). Penny et Hendy ont effectué une série d'analyses statistiques détaillées sur la signification des arbres phylogénétiques incongrus, et voici leur conclusion:
Pour un arbre phylogénétique universel plus réaliste avec des dizaines de taxons, y compris tous les phylums connus, la précision est meilleure de plusieurs ordres de grandeur. Pour mettre en perspective la signification de cette incroyable confirmation, considérons la théorie moderne de la gravité. La théorie de la gravitation universelle de Newton et la théorie de la relativité générale d'Einstein reposent toutes deux sur une constante physique fondamentale, G, la constante gravitationnelle. Si ces théories de la gravité sont correctes, des méthodes indépendantes devraient déterminer des valeurs similaires pour G. Cependant, à ce jour, des mesures indépendantes très précises de la constante de gravitation G ne concordent pas à près de 1% (Kestenbaum 1998; Quinn 2000). Voici comment David Kestenbaum décrit l’état scientifique actuel de la théorie de la gravité, publié dans la prestigieuse revue Science:
Plus de deux ans plus tard, le même Terry Quinn (du Bureau international des poids et mesures [BIPM] de Sèvres, en France) résumait la situation dans un article du journal Nature:
Néanmoins, une précision d'un peu moins de 1% reste assez bonne; En tout cas, elle est suffisante, à ce stade, pour ne pas de nous faire beaucoup douter de la validité et de l'utilité des théories modernes de la gravité. Cependant, si les tests de la théorie de la descendance commune donnaient des résultats médiocres, différents arbres phylogénétiques, comme le montre la figure 1, devraient différer de 18 branches sur 30 ! Dans leur quête de perfection scientifique, certains biologistes s'inquiètent à juste titre des divergences évidentes existant entre certains arbres phylogénétiques (Gura 2000; Patterson et al. 1993; Maley et Marshall 1998). Toutefois, comme illustré à la figure 1, l’arbre phylogénétique standard est connu avec 38 décimales, ce qui est une précision bien supérieure à celle des constantes physiques, même les mieux déterminées. À titre de comparaison, la charge de l'électron n'est connue qu'à sept décimales, la constante de Planck à huit décimales seulement, la masse du neutron, du proton et de l'électron ne sont connues qu'à neuf décimales et la gravitation universelle constante n’a été déterminée qu’à trois décimales.
De plus, si la descendance commune est vraie, nous nous attendons à ce que l'inclusion d'un plus grand nombre de données dans les analyses phylogénétiques augmente la correspondance entre les arbres phylogénétiques. Comme expliqué dans l'encadré sur les mises en garde phylogénétiques, les arbres à gènes ne sont pas équivalents aux arbres à espèces (Avise et Wollenberg, 1997; Fitch, 1970; Hudson, 1992; Nichols, 2001; Wu, 1991). La génétique et l'hérédité sont des processus stochastiques (c'est-à-dire probabilistes) et, par conséquent, nous nous attendons à ce que les phylogénies construites avec des gènes uniques soient partiellement incongrues. Cependant, l’inclusion de plusieurs gènes indépendants dans une analyse phylogénétique devrait permettre de contourner cette difficulté. En général, plus de cinq gènes indépendants sont nécessaires pour reconstruire avec précision la phylogénie d'une espèce (Wu, 1991). Les arbres phylogénétiques construits avec plusieurs gènes devraient donc être plus précis que ceux construits avec des gènes uniques, et les arbres de gènes combinés sont plus congruents (Baldauf et al. 2000; Hedges 1994; Hedges et Poling 1999; Penny et al. 1982).
Réfutation potentielle:
Lorsqu'il est devenu possible de séquencer des molécules biologiques, la réalisation d'un arbre très différent basé sur des preuves moléculaires indépendantes aurait porté un coup fatal à la théorie de l'évolution, bien que ce soit de loin le résultat le plus probable. Plus précisément, l'hypothèse de descendance commune aurait été réfutée si les arbres phylogénétiques universels déterminés à partir de preuves moléculaires et morphologiques indépendantes ne correspondaient pas de façon statistiquemente significative. De plus, nous sommes maintenant en mesure de commencer la construction d'arbres phylogénétiques basés sur d'autres lignes de données indépendantes, telles que l'organisation chromosomique. De manière très générale, le nombre et la longueur des chromosomes et la position chromosomique des gènes sont tous causalement indépendants de la morphologie et de l'identité de la séquence. Les phylogénie construites à partir de ces données devraient également récapituler l'arbre phylogénétique standard (Hillis et al. 1996; Li 1997).
Critiques:
Une objection commune est l’affirmation selon laquelle l’anatomie n’est pas indépendante de la biochimie et que, par conséquent, des organismes anatomiquement similaires sont susceptibles d’être biochimiquement similaires (par exemple dans leurs séquences moléculaires) simplement pour des raisons fonctionnelles. Selon cet argument, nous devrions donc nous attendre à ce que les phylogénie basées sur les séquences moléculaires soient similaires aux phylogénie basées sur la morphologie, même si les organismes ne sont pas apparentés par descendance commune. Cet argument est très faux. Il n'y a pas de raison biologique connue, en dehors de la descendance commune, de supposer que des morphologies similaires doivent avoir une biochimie similaire. Bien que cette logique puisse sembler tout à fait raisonnable au départ, toute la biologie moléculaire réfute cette corrélation de “bon sens”. En général, un ADN et une biochimie similaires donnent une morphologie et une fonction similaires, mais l'inverse n'est pas vrai: une morphologie et une fonction similaires ne sont pas nécessairement le résultat d'un ADN ou d'une biochimie similaires. La raison est facile à comprendre une fois expliquée; de nombreuses séquences d'ADN ou structures biochimiques très différentes peuvent avoir les mêmes fonctions et les mêmes morphologies (voir les prédictions 4.1 et 4.2 pour une explication détaillée).
Par analogie, considérons les programmes informatiques. Firefox fonctionne essentiellement de la même manière sur les ordinateurs Macintosh, IBM ou Unix, mais le code binaire de chaque programme est très différent. Les programmes informatiques qui remplissent les mêmes fonctions peuvent être écrits dans la plupart des langages informatiques: Basic, Fortran, C, C ++, Java, Pascal, etc. Des programmes identiques peuvent être compilés en code binaire de différentes manières. De plus, même en utilisant le même langage informatique, il existe de nombreuses façons différentes d’écrire un programme informatique spécifique, même en utilisant les mêmes algorithmes et routines. En fin de compte, il n'y a aucune raison de suspecter que des programmes informatiques similaires soient écrits avec un code similaire, basé uniquement sur la fonction du programme. C'est la raison pour laquelle les éditeurs de logiciels gardent leur code source secret, mais ils se soucient peu de savoir que les concurrents peuvent utiliser leurs programmes. Il est en principe impossible de déduire le code du programme de la fonction et du fonctionnement du logiciel. La même conclusion s’applique aux organismes biologiques, pour des raisons très similaires.
Pour réitérer, bien que des génotypes similaires (par exemple, des séquences moléculaires) donnent souvent des phénotypes similaires (par exemple, des caractères morphologiques), des phénotypes similaires ne sont pas nécessairement le résultat de génotypes similaires. Ainsi, il est tout à fait possible que des arbres phylogénétiques construits à partir de données génotypiques soient radicalement différents des arbres phylogénétiques construits à partir de données phénotypiques. En fait, en l'absence de descendance commune ou de toute autre raison de supposer que ces deux types d'arbres devraient être similaires, le résultat le plus probable est, de loin, qu'ils seront radicalement différents. C'est précisément pourquoi il est possible de réfuter la prédiction macro-évolutive selon laquelle les phylogénies déterminées indépendamment devraient être similaires.
Prédiction 1.4: Formes intermédiaires et transitoires: les morphologies possibles des ancêtres communs prédits
- Exemple 1: oiseaux - reptiles
- Exemple 2: mammifères- reptiles
- Exemple 3: singes humains
- Exemple 4: baleines à pattes
- Exemple 5: siréniens à pattes
Tous les animaux fossilisés trouvés doivent être conformes à l'arbre phylogénétique standard. Si tous les organismes sont unis par la descendance d'un ancêtre commun, il existe une seule et même véritable phylogénie historique pour tous les organismes. De même, il existe une seule véritable généalogie historique pour chaque être humain. Il s'ensuit directement que s'il existe une phylogénie universelle unique, tous les organismes, passés et présents, s'intègrent uniquement dans cette phylogénie. Puisque l'arbre phylogénétique standard est la meilleure approximation de la véritable phylogénie historique, nous nous attendons à ce que tous les animaux fossilisés se conforment à l'arbre phylogénétique standard dans l’intervalle d’erreur de nos méthodes scientifiques.
Chaque nœud partagé entre deux branches dans une phylogénie ou un cladogramme représente un ancêtre commun prédit; il y a donc environ 29 ancêtres communs prévus à partir de l'arbre illustré à la figure 1. Notre arbre standard montre que le groupe d'oiseaux est le plus étroitement lié au groupe reptilien, avec un nœud reliant les deux (A dans la figure 1); nous prévoyons donc la possibilité de trouver des intermédiaires fossiles entre les oiseaux et les reptiles. Le même raisonnement s'applique aux mammifères et aux reptiles (B dans la Figure 1). Cependant, nous prédisons que nous ne trouverons jamais d'intermédiaires fossiles entre oiseaux et mammifères.
Il convient de souligner que rien n’oblige les organismes intermédiaires à disparaître. En fait, tous les organismes vivants peuvent être considérés comme intermédiaires entre des taxons adjacents dans un arbre phylogénétique. Par exemple, les reptiles modernes sont intermédiaires entre les amphibiens et les mammifères, et les reptiles sont également intermédiaires entre les amphibiens et les oiseaux. En ce qui concerne les prédictions macroévolutives de la morphologie, ce point est trivial, car il s’agit essentiellement d’une simple reformulation du concept de hiérarchie imbriquée.
Cependant, un arbre phylogénétique fait des prédictions significatives sur la morphologie des intermédiaires qui n'existent plus ou qui n'ont pas encore été découverts. Chaque ancêtre commun prédit possède un ensemble de caractéristiques morphologiques explicitement spécifiées, basées sur chacun des caractères dérivés les plus courants de ses descendants et sur les transitions qui doivent avoir eu lieu pour transformer un taxon en un autre (Cunningham et al. 1998; Futuyma 1998, pp. 107-108). À partir de la connaissance de la morphologie aviaire et reptilienne, il est possible de prédire certaines des caractéristiques qu'un intermédiaire reptile-oiseau devrait avoir, le cas échéant. Par conséquent, nous nous attendons à la possibilité de trouver des fossiles ressemblant à des reptiles avec des plumes, à des oiseaux avec des dents ou à des oiseaux avec de longues queues de reptiles. Cependant, nous ne prévoyons pas de fossiles de transition entre oiseaux et mammifères, tels que des fossiles de mammifères avec des plumes ou des fossiles d'oiseaux avec des os d'oreille moyenne de type mammifère.
Confirmation:
Exemple 1 : oiseaux-reptiles Dans le cas qui vient d'être mentionné, nous avons trouvé un ensemble assez complet de fossiles de transition dinosaures à oiseaux sans “lacunes” morphologiques (Sereno 1999), représentés par Eoraptor, Herrerasaurus, Ceratosaurus, Allosaurus, Compsognathus, Sinosauropteryx, Protarchaeopteryx, Caudiptery, Velociraptor, Sinovenator, Beipiaosaurus, Sinornithosaurus, Microraptor, Archaeopteryx, Rahonavis, Confuciusornis, Sinornis, Patagopteryx, Hesperornis, Apsaravis, Ichthyornis et Columba, parmi beaucoup d'autres (Carroll 1997, p. 30; Xu et al., 1999; Xu et al., 2000; Xu et al., 2002). Tous ont les morphologies possibles attendues (voir la figure 3.1.1 de la prévision 3.1 pour quelques exemples), y compris des organismes tels que Protarchaeopteryx, Caudipteryx et le célèbre “BPM 1 3-13” (un dromaeosaure de Chine maintenant appelé Cryptovolans pauli; Czerkas et al. 2002) qui sont des dinosaures bipèdes, incapables de voler, avec des plumes de style moderne (Chen et al. 1998; Qiang et al. 1998; Norell et al. 2002). En outre, plusieurs dinosaures non volants similaires ont été découverts en étant recouverts de précurseurs évolutifs des plumes modernes (tégument ramifié en forme de plume impossible à distinguer du contour des plumes des vrais oiseaux), y compris Sinornithosaurus (“Bambiraptor”), Sinosauropteryx, Beipiaosaurus, Microraptor et un unnamed spécimen de dromaeosaur, NGMC 91, appelé de manière informelle “Dave” (Ji et al. 2001). La FAQ Tout sur Archaeopteryx donne une liste détaillée des différents caractères intermédiaires d’Archaeopteryx entre les reptiles et les oiseaux modernes.
Exemple 2 : Reptiles-mammifères
Nous avons également une série extrêmement complète de fossiles pour les intermédiaires reptiles-mammifères, allant des pelycosauria, therapsida, cynodonta jusqu’aux mammifères primitifs (Carroll 1988, p. 392-396; Futuyma 1998, p. 146-151; Gould 1990). Kardong 2002, pp. 255-275). Comme mentionné ci-dessus, l'arbre phylogénétique standard indique que les mammifères ont progressivement évolué à partir d'un ancêtre ressemblant à un reptile, et qu'il devait exister des espèces de transition morphologiquement intermédiaires entre les reptiles et les mammifères, bien qu'aucune ne soit vivante aujourd'hui. Cependant, il existe des différences morphologiques significatives entre les reptiles modernes et les mammifères modernes. Les os, bien sûr, sont ce qui se fossilise le plus facilement, et c’est là que nous recherchons des espèces de transition du passé. Sur le plan ostéologique, il existe deux différences majeures entre reptiles et mammifères: (1) les reptiles ont au moins quatre os dans la mâchoire inférieure (p. ex dentaires, articulaire, angulaires surangulaire et coronoïdes), tandis que les mammifères n'en ont qu'un (le dentaire), et (2) les reptiles ont seulement un os de l'oreille moyenne (l’étrier), tandis que les mammifères en ont trois (le marteau, l'enclume et l’étrier) (voir Figure 1.4.1).
Figure 1.4.1. Les mâchoires de trois vertébrés: le mammifère, le thérapside et le pelycosaure.
 Vue de côté de trois crânes idéalisés de mammifères, de thérapsidés (reptiles ressemblant à des mammifères) et de pelycosaures (jeunes reptiles). La figure montre les différences entre les mâchoires des mammifères et des reptiles et les structures osseuse de l’oreille. L'articulation de la mâchoire est représentée par un gros point noir, le quadratum (enclume de mammifère ou incus) est en bleu, l'articulaire (marteau ou malleus de mammifère) est en jaune et l’angulaire (tympan de mammifère) en rose. Notez comment, chez le reptile, l’articulation de la mâchoire est formée entre le quadratum bleu et l’articulaire jaune ( l’angulaire rose à proximité) et comment, chez le mammifère, l’articulation de la mâchoire se forme entre le squamosal en haut et le dentaire en dessous. Chez le reptile, le squamosal est juste au-dessus et entre en contact avec le quadratum. Les thérapides avancées ont deux articulations de la mâchoire: une articulation de reptile et une articulation de mammifère (Figure basée sur Kardong 2002, p. 275, reproduite avec l'autorisation de l'éditeur, Copyright © 2002 McGraw-Hill).
Vue de côté de trois crânes idéalisés de mammifères, de thérapsidés (reptiles ressemblant à des mammifères) et de pelycosaures (jeunes reptiles). La figure montre les différences entre les mâchoires des mammifères et des reptiles et les structures osseuse de l’oreille. L'articulation de la mâchoire est représentée par un gros point noir, le quadratum (enclume de mammifère ou incus) est en bleu, l'articulaire (marteau ou malleus de mammifère) est en jaune et l’angulaire (tympan de mammifère) en rose. Notez comment, chez le reptile, l’articulation de la mâchoire est formée entre le quadratum bleu et l’articulaire jaune ( l’angulaire rose à proximité) et comment, chez le mammifère, l’articulation de la mâchoire se forme entre le squamosal en haut et le dentaire en dessous. Chez le reptile, le squamosal est juste au-dessus et entre en contact avec le quadratum. Les thérapides avancées ont deux articulations de la mâchoire: une articulation de reptile et une articulation de mammifère (Figure basée sur Kardong 2002, p. 275, reproduite avec l'autorisation de l'éditeur, Copyright © 2002 McGraw-Hill).
Au début du 20ème siècle, les biologistes du développement ont découvert quelque chose qui complique davantage la situation. Chez le fœtus reptilien, deux os de la tête en développement forment finalement deux os dans la mâchoire reptilienne inférieure, le quadratum et l'articulaire (voir le Pelycosaure à la figure 1.4.1). De manière surprenante, les os en développement correspondants chez le fœtus de mammifère forment finalement l'enclume et le marteau de l'oreille moyenne de mammifère (également connus plus officiellement sous le nom d'incus et de malleus, respectivement; voir la figure 1.4.2) (Gilbert 1997, p. 894-896). ). Ces faits indiquaient clairement que le marteau et l'enclume avaient évolué à partir de ces mâchoires reptiliennes, si la descendance commune était vraie. Ce résultat était si frappant et les intermédiaires requis si bizarres que de nombreux anatomistes avaient bien du mal à imaginer comment des formes transitionnelles reliant ces morphologies auraient pu exister tout en conservant leur fonction. Duane Gish, créationniste de la Terre-jeune, a formulé le problème de la manière suivante:
Figure 1.4.2. Une comparaison des oreilles des reptiles et des mammifères.

 L'oreille de reptile est montrée à gauche, l'oreille de mammifère à droite. Comme sur la figure 1.4.1, le quadratum (enclume ou incus de mammifère) est en bleu et l’articulaire (marteau ou malleus de mammifère) en jaune. L’étrier est montré en marron. Notez comment la disposition relative de ces os est similaire chez les deux taxons, dans l'ordre suivant: oreille interne-étrier-quadratum-articulaire.
L'oreille de reptile est montrée à gauche, l'oreille de mammifère à droite. Comme sur la figure 1.4.1, le quadratum (enclume ou incus de mammifère) est en bleu et l’articulaire (marteau ou malleus de mammifère) en jaune. L’étrier est montré en marron. Notez comment la disposition relative de ces os est similaire chez les deux taxons, dans l'ordre suivant: oreille interne-étrier-quadratum-articulaire.
Gish avait tort d'affirmer qu'il n'y avait aucune forme fossile de transition et il a été repris sur cette gaffe plusieurs fois depuis qu'il a écrit ces mots. Cependant, les déclarations de Gish définissent bien le problème morphologique à résoudre. Passons en revue la conclusion évolutive requise. Au cours de leur évolution, deux os de mammifère de l'oreille moyenne (le marteau et l'enclume, alias malleus et l'incus) ont dérivés de deux mâchoires reptiliennes. Ainsi, il y avait une transition évolutive majeure dans laquelle plusieurs os de la mâchoire reptiliens (le quadrate, l’articulaire et l’angulaire) ont été considérablement réduits et modifiés progressivement pour former l'oreille moyenne des mammifères modernes. Dans le même temps, l'os dentaire, une partie de la mâchoire reptilienne, a été élargi pour former l'os maxillaire inférieur du mammifère. Au cours de ce changement, les os qui forment la charnière de la mâchoire ont changé d'identité. Il est important de noter que l'articulation de la mâchoire reptilienne est formée à l'intersection du quadrat et de l'articulaire, tandis que l'articulation de la mâchoire des mammifères est formée à l'intersection du squamosal et du dentaire (voir Figure 1.4.1).
Comment préserver l'audition et l'articulation de la mâchoire pendant cette transition? Comme le montrent clairement les nombreux fossiles de transition découverts (voir figure 1.4.3), les os qui transmettent le son dans l'oreille des reptiles et des mammifères ont été en contact tout au long de l'évolution de cette transition. Chez les reptiles, l’étrier entre en contact avec le quadratum, qui à son tour entre en contact avec l'articulaire. Chez les mammifères, l’étrier entre en contact avec l'incus, qui à son tour entre en contact avec le malleus (voir figure 1.4.2). Depuis que le quadratum a évolué en incus et que l’articulaire a évolué en malleus, ces trois os ont été en contact constant pendant ce changement évolutif impressionnant. De plus, une articulation de la mâchoire fonctionnelle a été maintenue par redondance: plusieurs fossiles intermédiaires possèdent une articulation de la mâchoire reptilienne (du quadratum et articulaire) et une articulation de la mâchoire de mammifère (du dentaire et du squamosal). Plusieurs cynodontes tardifs et Morganucodon ont clairement une mâchoire à double articulation. De cette manière, l'articulation de la mâchoire de type reptilien était libérée pour évoluer vers une nouvelle fonction spécialisée dans l'oreille moyenne. Il est à noter que certaines espèces modernes de serpents ont une mâchoire à double articulation impliquant différents os, de sorte qu'un tel arrangement mécanique est certainement possible et fonctionnel.
Depuis la création de la figure 1.4.3, plusieurs fossiles intermédiaires importants ont été découverts et s’adaptent entre Morganucodon et les premiers mammifères. Ces nouvelles découvertes comprennent un crâne complet de Hadrocodium wui (Luo et al. 2001) et du matériel crânien et maxillaire de Repenomamus et Gobiconodon (Wang et al. 2001). Ces nouvelles découvertes de fossiles clarifient exactement quand et comment le malleus, l’incus et l’angulaire se sont complètement détachés de la mâchoire inférieure et sont devenus des osselets de l’oreille.
Rappelons-nous que Gish a déclaré: “Il n’existe aucune forme fossile de transition montrant, par exemple, trois ou deux os de la mâchoire, ou deux os de l’oreille” (Gish, 1978, p. 80). Gish ne comprend tout simplement pas comment se produisent les transitions graduelles (quelque chose qu'il devrait comprendre, évidemment, s'il a l'intention de critiquer la théorie de l'évolution). Ces intermédiaires fossiles illustrent en quoi la déclaration de Gish est une description erronée de l'apparence d'une forme transitoire. Dans plusieurs des intermédiaires connus, les os ont des fonctions qui se chevauchent, et un os peut être appelé à la fois os de l'oreille et os de la mâchoire; ces os remplissent deux fonctions. Ainsi, il n'y a aucune raison de s'attendre à des formes de transition avec un nombre intermédiaire d'os de la mâchoire ou de l'oreille. Par exemple, chez Morganucodon, le quadratum (enclume) et l’articulaire (marteau) servent simultanément d’os d’oreille de mammifère et d’os de mâchoire reptilienne. En fait, même chez les reptiles modernes, le quadratum et l'articulaire servent à transmettre le son aux étriers et à l'oreille interne (voir Figure 1.4.2). La transition pertinente est donc un processus par lequel les os de l'oreille, initialement situés dans la mâchoire inférieure, se spécialisent dans leur fonction en se détachant de la mâchoire inférieure et en se rapprochant de l'oreille interne.
Figure 1.4.3. Une comparaison des os de la mâchoire et des os de l'oreille de plusieurs formes de transition dans l'évolution des mammifères
 Les plages stratigraphiques approximatives des différents taxons sont indiquées à l'extrême gauche (plus récentes en haut). La colonne gauche des mâchoires montre la vue de la mâchoire gauche de l'intérieur de la bouche. La colonne de droite représente la vue de l'os maxillaire droit du côté droit (à l'extérieur du crâne). Comme sur la figure 1.4.1, le quadratum (enclume ou incus de mammifère) est en bleu, l’articulaire (marteau ou malleus de mammifère) est en jaune et l’angulaire (tympan de mammifère) en rose. Par souci de clarté, les dents ne sont pas montrées et l'os de la mâchoire supérieure squamosal est omis (il remplace le quadratum dans l'articulation de la mâchoire de mammifère et fait partie de l'articulation de la mâchoire chez les cynodontes avancés et Morganucodon). Q = quadratum, Ar = articulaire, An = angulaire, I = incus (enclume), Ma = malleus (marteau), Ty = tympan, D = dentaire. (Reproduit de Kardong 2002, p. 274, avec la permission de l'éditeur, Copyright © 2002 McGraw-Hill)
Les plages stratigraphiques approximatives des différents taxons sont indiquées à l'extrême gauche (plus récentes en haut). La colonne gauche des mâchoires montre la vue de la mâchoire gauche de l'intérieur de la bouche. La colonne de droite représente la vue de l'os maxillaire droit du côté droit (à l'extérieur du crâne). Comme sur la figure 1.4.1, le quadratum (enclume ou incus de mammifère) est en bleu, l’articulaire (marteau ou malleus de mammifère) est en jaune et l’angulaire (tympan de mammifère) en rose. Par souci de clarté, les dents ne sont pas montrées et l'os de la mâchoire supérieure squamosal est omis (il remplace le quadratum dans l'articulation de la mâchoire de mammifère et fait partie de l'articulation de la mâchoire chez les cynodontes avancés et Morganucodon). Q = quadratum, Ar = articulaire, An = angulaire, I = incus (enclume), Ma = malleus (marteau), Ty = tympan, D = dentaire. (Reproduit de Kardong 2002, p. 274, avec la permission de l'éditeur, Copyright © 2002 McGraw-Hill)
Exemple 3: singes-humains
Gottfried Wilhelm Leibniz
Protogaea 1749
L'un des exemples les plus célèbres de fossiles de transition est notre collection d'hominidés fossiles (voir la figure 1.4.4 ci-dessous). Basé sur le consensus de nombreuses analyses phylogénétiques, Pan troglodytes (le chimpanzé) est le plus proche parent vivant de l'homme. Nous nous attendons donc à ce que des organismes ayant une morphologie intermédiaire entre l’homme et le chimpanzé aient vécu dans le passé. Au cours du siècle dernier, de nombreuses découvertes paléontologiques spectaculaires ont permis d'identifier de tels fossiles de transition d'hominidés.
Figure 1.4.4. Crânes d'hominidés fossiles
- (A) Pan troglodytes, chimpanzé, moderne
- (B) Australopithecus africanus, STS 5, 2.6 Ma
- (C) Australopithecus africanus, STS 71, 2.5 Ma
- (D) Homo habilis, KNM-ER 1813, 1.9 Ma
- (E) Homo habilis, OH24, 1.8 Ma
- (F) Homo rudolfensis, KNM-ER 1470, 1.8 Ma
- (G) Homo erectus, Dmanisi cranium D2700, 1.75 Ma
- (H) Homo ergaster (early H. erectus), KNM-ER 3733, 1.75 Ma
- (I) Homo heidelbergensis, ”Rhodesia man,“ 300,000 – 125000 a
- (J) Homo sapiens neanderthalensis, http://www.mnh.si.edu/anthro/humanorigins/ha/laferr.html|La Ferrassie]] 1, 70 000 a
- (K) Homo sapiens neanderthalensis, La Chappelle-aux-Saints, 60 000 a
- (L) Homo sapiens neanderthalensis, Le Moustier, 45 000 a
- (M) Homo sapiens sapiens, Cro-Magnon I, 30 000 a
- (N) Homo sapiens sapiens, moderne
(Images © 2000 Smithsonian Institution)
Exemple 4: baleines fossiles à pattes
Michael J. Behe
Anti-darwinien, théoricien du design intelligent,
écrivant contre la validité de l'évolution moins d'un an avant que trois espèces de transition entre les baleines et les mésonychidées terrestres de l’Eocène soient trouvées.
Un autre exemple impressionnant de formes de transition incontestables, prédits par les biologistes de l'évolution, est la collection d'intermédiaires fossiles entre les mammifères terrestres et les baleines. Les baleines, bien sûr, sont des animaux marins avec des nageoires, sans membres postérieurs externes. Comme ils sont aussi des mammifères, la phylogénie standard indique que les baleines et les dauphins ont évolué à partir de mammifères terrestres avec des pattes. Ces dernières années, nous avons trouvé plusieurs formes de transition de baleines à pattes, à la fois capables et incapables de locomotion terrestre (Gingerich et al. 1983; Gingerich et al. 1990; Gingerich et al. 1994; Gingerich et al. 2001; Thewissen et al. 2001).
Exemple 5 : Siréniens à pattes
Figure 1.4.5. Un fossile sirénien intermédiaire: une sirène avec des jambes.
Les Siréniens (lamantins et dugongs) sont des mammifères entièrement aquatiques avec des nageoires pour les membres antérieurs et aucun membre postérieur. La théorie évolutionniste prédit que les siréniens ont évolué à partir d’ancêtres terrestres, et que nous trouverions des intermédiaires à pattes. Récemment, un nouveau fossile de transition a été découvert en Jamaïque, un sirénien à quatre pattes (Domning, 2001).
Il existe de nombreux autres exemples tels que ceux-ci - la plupart peuvent être trouvés dans l'excellente FAQ sur les fossiles intermédiaire de vertébrés.
Réfutation potentielle:
Toute découverte d'un intermédiaire frappant mi-mammifère, mi-oiseau serait hautement incompatible avec une descendance commune. On peut penser à de nombreux autres exemples d'intermédiaires interdits, basés sur l'arbre standard (Kemp 1982; Stanley 1993; Carroll 1997; Chaterjee 1997).
Un point subtil, mais important, est qu'une interprétation évolutionniste cladistique stricte exclut la possibilité d'identifier de vrais ancêtres; seuls les intermédiaires ou les transitoires peuvent être identifiés positivement. (Pour les besoins de cet article, transitoires et intermédiaires sont considérés comme synonymes.) La seule preuve irréfutable d'une relation ancêtre-descendant est l'observation d'une naissance; évidemment ceci est normalement plutôt improbable dans le registre fossile. Les intermédiaires ne sont pas nécessairement exactement identiques aux ancêtres prédits; en fait, il est plutôt improbable qu'ils soient identiques. Simplement pour des raisons de probabilité, les intermédiaires que nous découvrons ne seront probablement pas les véritables ancêtres d'une espèce moderne, mais seront étroitement liés à un ancêtre commun prédit. Par conséquent, les intermédiaires que nous trouvons auront probablement des caractères dérivés supplémentaires en plus des caractères qui les ont identifiés comme intermédiaires. En raison de ces considérations, lors de la découverte d’une nouvelle et importante espèce de fossile intermédiaire, les paléontologues prudents préciserons souvent que l’espèce intermédiaire à l’étude n’est probablement pas un ancêtre, mais est plutôt “représentative d’un ancêtre commun” ou est une “branche évolutive secondaire”. Moins il y a de caractères extravagants dans un fossile intermédiaire, plus il est probable qu'un fossile intermédiaire devienne un véritable ancêtre. Pour plus de précisions, voir la prédiction 5.4.
Prédiction 1.5: Ordre chronologique des intermédiaires
Les intermédiaires fossilisés doivent apparaître dans le bon ordre chronologique général en fonction de l’arbre standard. Tout arbre phylogénétique prédit un ordre chronologique relatif de l'évolution d'ancêtres hypothétiques communs et d'intermédiaires entre ces ancêtres. Par exemple, dans notre exemple actuel, l'ancêtre commun reptile-mammifère (B) et leurs intermédiaires devraient être plus vieux que l'ancêtre commun reptile-oiseaux (A) et leurs intermédiaires.
Il convient toutefois de noter qu’il existe un certain “jeu” dans les contraintes temporelles imposées par toute phylogénie, et ce pour deux raisons principales: (1) la confiance statistique (ou l’erreur) associée à une phylogénie et à ses branches internes spécifiques, et ( 2) la résolution inhérente des archives fossiles (résultant en dernier ressort des aléas du processus de fossilisation). Comme mentionné précédemment, la plupart des arbres phylogénétiques ont des branches hautement fiables, car elles sont bien étayées par les données, et d'autres branches dans lesquelles nous avons moins confiance, car elles sont statistiquement moins significatives et mal étayées par les données. Voir également les mises en garde associées à l'analyse phylogénétique.
Lors de l’évaluation de l’ordre géologique des fossiles, rappelez-vous qu’une fois l’espèce en transition apparue, il n’y a aucune raison pour laquelle elle doit disparaitre et être remplacée. Par exemple, dans de rares cas, certains organismes n’ont subi que peu de changements au cours de 100 à 200 millions d’années. Quelques exemples connus sont les “fossiles vivants”, tels que le cœlacanthe, qui dure depuis environ 80 millions d'années; la chauve-souris, qui n'a pas beaucoup changé depuis 50 millions d'années; et même l'écureuil moderne, qui n'a pas changé depuis 35 millions d'années. En fait, les études paléontologiques indiquent que la longévité moyenne de 21 familles vivantes de vertébrés est d’environ 70 millions d’années (Carroll 1997, p. 167).
De plus, les archives fossiles sont manifestement incomplètes; les espèces apparaissent dans les archives fossiles, puis disparaissent, puis réapparaissent plus tard. Le cœlacanthe, qui figurait pour la dernière fois dans les archives fossiles il y a 80 millions d'années, mais encore vivant aujourd'hui, constitue un cas exceptionnel. Durant le Crétacé (période critique dans l'évolution des oiseaux), il existe 50 million d’années d'écart dans l’enregistrement du diplodocoidean, supérieur à 40 millions d'années dans le cas du pachycéphalosaure, supérieur à 20 millions d'années pour le trodontidiae. et un fossé d'environ 15 millions d'années dans les fossiles d'oviraptosauriens (ces deux derniers ordres de dinosaures sont des théropodes maniraptoriens cœlurosauriens, qui jouent un rôle important dans l'évolution des oiseaux). Pendant le Jurassique, il existe un fossé de 40 millions d'années dans les archives fossiles des hétérodontosauridés (Sereno 1999). La plupart des organismes ne se fossilisent pas et rien n'oblige à trouver un représentant de chaque espèce dans les archives fossiles. Comme le savent tous les étudiants diplômés en recherche scientifique (ou apprennent éventuellement à la dure), les arguments fondés sur des preuves négatives sont des arguments scientifiques très faibles, en particulier en l'absence de contrôles positifs appropriés. Ainsi, sur la base des restes fossiles d'espèces modernes et des lacunes actuelles connues dans les archives paléontologiques d'espèces éteintes, l'observation d'espèces en transition “à la mauvaise place” de 40 millions d'années devrait être assez courante. Ce degré de “jeu” dans les archives fossiles est en réalité plutôt mineur, si l’on considère que les archives fossiles de la vie durent entre 2 et 3,8 milliards d’années et que celles des organismes multicellulaires couvrent un total d’environ 660 millions d’années. Une incertitude de 40 millions d'années équivaut à une erreur relative d'environ 1% ou 6%, respectivement – donc plutôt faible.
Confirmation :
Les intermédiaires oiseaux-reptiles mentionnés ci-dessus datent du Jurassique supérieur et du Crétacé inférieur (il y a environ 150 millions d'années), alors que pelycosauria et therapsida (intermédiaires reptiles-mammifères) sont plus anciens et datent du Carbonifère et du Permien (environ 250 à 350 millions d'années). voir l’échelle de temps géologique). C’est précisément ce qu’il faut observer si les archives fossiles correspondent à l’arbre phylogénétique standard.
La méthode la plus rigoureuse sur le plan scientifique pour confirmer cette prévision consiste à démontrer une corrélation positive entre phylogénie et stratigraphie, c'est-à-dire une corrélation positive entre l'ordre des taxons dans un arbre phylogénétique et l'ordre géologique dans lequel ces taxons apparaissent pour la première et dernière fois (que ce soit des intermédiaires vivants ou éteints). Par exemple, dans l’intervalle d'erreur inhérente aux archives fossiles, les procaryotes devraient apparaître en premier, suivis des simples animaux multicellulaires tels que les éponges et les étoiles de mer, puis les lamproies, les poissons, les amphibiens, les reptiles, les mammifères, etc., comme le montre la Figure 1. Contreirement aux opinions erronées (et non référencées) de certains anti-évolutionnistes (par exemple, Wise 1994, p. 225-226), les études des dix dernières années sur cette question ont confirmé l'existence d'une corrélation positive entre phylogénie et stratigraphie, avec une signification statistique (Benton 1998; Benton and Hitchin 1996; Benton and Hitchin 1997; Benton et al. 1999; Benton et al. 2000; Benton and Storrs 1994; Clyde and Fisher 1997; Hitchin and Benton 1997; Huelsenbeck 1994; Norell and Novacek 1992a; Norell and Novacek 1992b; Wills 1999). En utilisant trois mesures différentes de corrélation phylogénie-stratigraphie [RCI, GER et SCI (logiciel Ghosts 2.4, Wills 1999)], une corrélation positive élevée a été trouvée entre l'arbre phylogénétique standard décrit à la figure 1 et la plage stratigraphique des mêmes taxons, avec une signification statistique très élevée (P <0,0001) (ce travail, fichier d’entrée Ghosts disponible sur demande).
Un autre exemple spécifique, une première analyse publiée dans Science par Mark Norell et Michael Novacek (Norell et Novacek 1992b) a examiné 24 taxons de vertébrés différents (téléostéens, amniotes, reptiles, synapsides, diapsides, lépidosaures, squamates, deux ordres de dinosaures, deux ordres d'hadrosaures, pachycéphalées, mammifères supérieurs, primates, rongeurs, ongulés, artiodactyles, ruminants, éléphantiformes, brontotheres, tapiroidés, chalicotheres, Chalicotheriinae et équidés). Pour chaque taxon, la position phylogénétique de fossiles connus a été comparée à la position stratigraphique des mêmes fossiles. Une corrélation positive a été trouvée pour l'ensemble des 24 taxons, dont 18 étaient statistiquement significatifs.
Troisième exemple, Michael Benton et Rebecca Hitchin ont publié une analyse stratigraphique plus récente, grandement plus développée et détaillée de 384 cladogrammes publiés de divers organismes multicellulaires (Benton et Hitchin, 1997). En utilisant trois mesures de congruence entre les archives fossiles et la phylogénie (RCI, SRC et SCI), ces chercheurs ont observé des valeurs “tellement divergents d’une distribution normale [c'est-à-dire du hasard] qu'elles prouvent la forte congruence des deux ensembles de données [fossiles et cladogrammes]. ” En outre, l'analyse de Benton et Hitchin était extrêmement conservatrice, puisqu'elle ne faisait aucun effort pour exclure les cladogrammes avec une résolution médiocre, pour exclure les cladogrammes avec un très petit nombre de taxons ou pour n'utiliser que des fossiles avec des dates fiables. L'inclusion de ce types de données ajoute des éléments aléatoires à l'analyse et réduit la concordance apparente entre la stratigraphie et les cladogrammes. Malgré tout, les résultats étaient dans l’ensemble extrêmement statistiquement significatifs (p <0,0005). Comme les auteurs le commentent dans leur discussion:
De plus, si la corrélation entre la phylogénie et la stratigraphie est due à la descente commune, on pourrait s’attendre à ce que la corrélation s’améliore sur des périodes géologiques plus longues (étant donné que l’erreur relative associée aux archives fossiles diminue). Ceci a été observé (Benton et al. 1999). Nous nous attendions également à ce que la corrélation s'améliore et ne s'aggrave pas à mesure que davantage de fossiles sont découverts, ce qui a également été observé (Benton et Storrs, 1994).
Réfutation potentielle:
Il serait très incohérent que l'ordre chronologique soit inversé chez les exemples reptile-oiseau et reptile-mammifère. Même la découverte d’une absence de corrélation globale entre la stratigraphie et la phylogénie consensuelle des principaux taxons serait très problématique pour la théorie de la descendance commune. En outre, la corrélation observée pourrait diminuer sur de plus longues périodes ou à mesure que nous obtenons davantage de données paléontologiques, mais ce n'est pas le cas (Benton et al. 1999; Benton et Storrs 1994).
Compte tenu de la confiance élevée dans certaines branches des arbres phylogénétiques, certaines contraintes temporelles sont extrêmement rigides. Par exemple, nous ne devrions jamais trouver de fossiles mammifères ou aviaires dans ou avant les dépôts dévoniens, avant que les reptiles se soient éloignés de la lignée des tétrapodes amphibiens. Cela exclut les gisements précambriens, cambriens, ordoviciens et siluriens, qui représentent 92% de l'histoire géologique de la Terre et 65% de l'histoire biologique des organismes multicellulaires. Même une découverte incontestable de tout mammifère, oiseau ou fleur antérieur au Dévonien briserait la théorie de la descendance commune (Kemp 1982; Carroll 1988; Stanley 1993; Chaterjee 1997).
Références
- Albert, J., Wahlberg, J., Leitner, T., Escanilla, D. and Uhlen, M. (1994) “Analysis of a rape case by direct sequencing of the human immunodeficiency virus type 1 pol and gag genes.” J Virol 68: 5918-24. PubMed
- Archie, J. W. (1989) “A randomization test for phylogenetic information in systematic data.” Systematic Zoology 38: 219-252.
- Arnold, C., Balfe, P. and Clewley, J. P. (1995) “Sequence distances between env genes of HIV-1 from individuals infected from the same source: implications for the investigation of possible transmission events.” Virology 211: 198-203. PubMed
- Atchely, W. R., and Fitch, W. M. (1991) “Gene trees and the origins of inbred strains of mice.” Science 254: 554-558. PubMed
- Avery, O. T., MacLeod, C. M. and McCarty, M. (1944) “Studies on the chemical nature of the substance inducing transformation of pneumococcal types.” J. Exp. Med. 79:137-158.
- Avise, J. C., and Wollenberg, K. (1997) “Phylogenetics and the origin of species.” PNAS 94: 7748-7755. http://www.pnas.org/cgi/ content/full/94/15/7748
- Bailey, T. L., and Gribskov, M. (1998) “Combining evidence using p-values: application to sequence homology searches. Bioinformatics. 14: 48-54. PubMed
- Bajpai, S. and Gingerich, P. D. (1998) “A new Eocene archaeocete (Mammalia, Cetacea) from India and the time of origin of whales.” Proc Natl Acad Sci U S A. 95: 15464-15468. PubMed
- Baldauf, S. L., Roger, A. J., Wenk-Siefert, I., and Doolittle, W. F. (2000) “A kingdom-level phylogeny of eukaryotes based on combined protein data.” Science 290: 972-7. PubMed
- Behe, M.J. (1994) “Experimental support for regarding functional classes of proteins to be highly isolated from each other.” In Darwinism, Science or Philisophy? Eds. Jon Buell and Virginia Hearn, Foundation for Thought and Ethics: Houston, Texas. ARN Michael Behe Files
- Benton, M. J. (1998) “Molecular and morphological phylogenies of mammals: Congruence with stratigraphic data.” Molecular Phylogenetics and Evolution 9: 398-407. PubMed
- Benton, M. J., and Hitchin, R. (1996) “Testing the quality of the fossil record by groups and by major habitats.” Historical Biol. 12: 111-157.
- Benton, M. J., and Hitchin, R. (1997) “Congruence between phylogenetic and stratigraphic data on the history of life.” Proc. R. Soc. Lond. B. 264: 885-890.
- Benton, M. J., Hitchin, R., and Wills, M. A. (1999) “Assessing congruence between cladistic and stratigraphic data.” Syst. Biol. 48: 581-596.
- Benton, M. J., and Storrs, G. W. (1994) “Testing the quality of the fossil record: paleontological knowledge is improving.” Geology 22: 111-114.
- Benton, M. J., Wills, M. A., and Hitchin, R. (2000) “Quality of the fossil record through time.” Nature 403: 534-537. PubMed
- Birch, C. J., McCaw, R. F., Bulach, D. M., Revill, P. A., Carter, J. T., Tomnay, J., Hatch, B., Middleton, T. V., Chibo, D., Catton, M. G., Pankhurst, J. L., Breschkin, A. M., Locarnini, S. A. and Bowden, D. S. (2000) “Molecular analysis of human immunodeficiency virus strains associated with a case of criminal transmission of the virus.” J Infect Dis 182: 941-4. http://www.journals.uchicago.edu/JID/journal/issues/v182n3/000154/000154.html
- Blanchard, A., Ferris, S., Chamaret, S., Guetard, D. and Montagnier, L. (1998) “Molecular evidence for nosocomial transmission of human immunodeficiency virus from a surgeon to one of his patients.” J Virol 72: 4537-40. http://jvi.asm.org/cgi/content/full/72/5/4537?view=full&pmid=9557756
- Box, G. E. P. (1978) Statistics for experimenters : an introduction to design, data analysis, and model building. New York: John Wiley and Sons.
- Brenner, S. (1957) “On the impossibility of all overlapping triplet codes in information transfer from nucleic acid to proteins.” PNAS 43:687-694.
- Brown, J. R., Douady, C. J., Italia, M. J., Marshall, W. E., and Stanhope, M. J. (2001) “Universal trees based on large combined protein sequence data sets.” Nature Genetics 28: 281-285. PubMed
- Bryant, D., MacKenzie, A. and Steel, M. (2002). “The size of a maximum agreement subtree for random binary trees.” In: Bioconsensus II. DIMACS Series in Discrete Mathematics and Theoretical Computer Science (American Mathematical Society). ed., M.F. Janowitz.
- Carroll, R. L. (1988) Vertebrate Paleontology and Evolution. New York: W. H. Freeman and Co.
- Carroll, R. L. (1997) Patterns and Processes of Vertebrate Evolution. Cambridge: Cambridge University Press.
- Carter, G. S. (1954) Animal Evolution. London: Sidgwick and Jackson.
- Czerkas, S.A., Zhang, D., Li, J. and Li, Y. (1954) “Flying dromaeosaurs.” Dinosaur Museum Journal 1:97-126.
- Chaterjee, S. (1997) The Rise of Birds: 225 million years of evolution. Baltimore, MD: Johns Hopkins University Press.
- Chen, P.-j., Z.-m. Dong, et al. (1998) “An exceptionally well-preserved theropod dinosaur from the Yixian formation of China.” Nature 391: 147-152.
- Clyde, W. C., and Fisher, D. C. (1997) “Compaing the fit of stratigraphic and morphologic data in phylogenetic analysis.” Paleobiology 23: 1-19.
- Crick, F. H. C., Barnett, L., Brenner, S., and Watts-Tobin, R. J. (1961) “General nature of the genetic code for proteins.” Nature 192:1227-1232.
- Crick, F. H. C. and Orgel, L. E. (1973) “Directed panspermia.” Icarus 19:341-346.
- Cunningham, C. W., Omland, K. E., and Oakley, T. H. (1998) “Reconstructing ancestral character states: a critical reappraisal.” Trends in Ecology and Evolution 13: 361-366.
- Darwin, C. (1872) The Origin of Species. Sixth Edition. The Modern Library, New York. Project Gutenberg text file
- Dickerson, R. E., and Timkovich, R. (1975) cytochrome c. The Enzymes. P. D. Boyer. New York: Academic Press. 11: 397-547.
- Dodson, E. O. (1960) Evolution: Process and Product. New York: Reinhold Publishers.
- Domning, D. P. (2001) “The earliest known fully quadrupedal sirenian.” Nature. 413: 625-627. PubMed
- Doolittle, W. F. (1999) “Phylogenetic Classification and the Universal Tree.” Science 284: 2124. PubMed
- Doolittle, W. F. (2000) “The nature of the universal ancestor and the evolution of the proteome.” Current Opinion in Structural Biology 10: 355-358. PubMed
- Faith, D. P., and Cranston, P. S. (1991) “Could a cladogram this short have arisen by chance alone?: on permutation tests for cladistic structure.” Cladistics 7: 1-28.
- Farris, J. S. (1989) “The retention index and the rescaled consistency index.” Cladistics 5:417-419.
- Felsenstein, J. (1982) “Numerical methods for inferring evolutionary trees.” Quart. Rev. Biol. 57: 379-404.
- Felsenstein, J. (1985) “Confidence limits on phylogenies: an approach using the bootstrap.” Evolution 39: 783-791.
- Fisher, R. A. (1990) Statistical methods, experimental design, and scientific inference. Bennet, J. H. ed., Oxford: Oxford University Press.
- Fitch, W. M. (1970) “Distinguishing homologous from analogous proteins.” Syst. Zool. 28: 132-163.
- Futuyma, D. (1998) Evolutionary Biology. Third edition. Sunderland, MA: Sinauer Associates.
- Galton, F. and Watson, H.W. (1874) “On the probability of the extinction of families.” Journal of the Royal Anthropological Institute 4: 138-144.
- Garavelli, J. S., Hou, Z., et al. (2001) “The RESID Database of protein structure modifications and the NRL-3D Sequence-Structure Database.” Nucleic Acids Research 29: 199-201. http://www.ncifcrf.gov/RESID/
- Gish, D. T. (1978) Evolution? The Fossils Say No! Public School Edition, San Diego: Creation-Life Publishers.
- Gilbert, S. F. (1997) Developmental Biology. Fifth edition. Sinauer Associates.
- Gingerich, P., Wells, N. A., Russell, D. E., and Shah, S. M. I. (1983) “Origin of whales in epicontinental remnant seas: new evidence from the early Eocene of Pakistan.” Science 220: 403-406.
- Gingerich, P., Smith, B. H., and Simons, E. L. (1990) “Hind limbs of Eocene Basilosaurus: evidence of feet in whales.” Science 249: 154-157.
- Gingerich, P., Raza, S. M., Arif, M., Anwar, M., and Zhou, X. (1994) “New whale from the Eocene of Pakistan and the origin of cetacean swimming.” Nature 368: 844-847.
- Gingerich, P. D., Haq Mu, Zalmout, I. S., Khan, I. H., and Malkani, M. S. (2001). “Origin of whales from early artiodactyls: hands and feet of Eocene Protocetidae from Pakistan.” Science. 293: 2239-2242. PubMed
- Givnish, T.J., and Sytsma, K.J. (1997) “Consistency, characters, and the likelihood of correct phylogenetic inference.” Mol Phylogenet Evol. 7: 320-330. PubMed
- Goujon, C. P., Schneider, V. M., Grofti, J., Montigny, J., Jeantils, V., Astagneau, P., Rozenbaum, W., Lot, F., Frocrain-Herchkovitch, C., Delphin, N., Le Gal, F., Nicolas, J. C., Milinkovitch, M. C. and Deny, P. (2000) “Phylogenetic analyses indicate an atypical nurse-to-patient transmission of human immunodeficiency virus type 1.” J Virol 74: 2525-32. http://jvi.asm.org/cgi/content/full/74/6/2525?view=full&pmid=10684266
- Gould, S. J. (1990) “An earful of jaw.” Natural History 3: 12-23.
- Gregory, W. K. (1951) Evolution Emerging: A survey of changing patterns from primeval life to man. Volume I. The Macmillan Co., New York.
- Groves, C. P. (2000) “The genus Cheirogaleus: Unrecognized biodiversity in dwarf lemurs.” International Journal of Primatology. 21(6): 943-962.
- Gura, T. (2000) “Bones, molecules … or both?” Nature 406: 230-233. PubMed
- Haeckel, E. (1898) The Last Link. London: Adam and Charles Black.
- Harris, T. E. (1989) The Theory of Branching Processes. New York: Dover.
- Hedges, S. B. (1994) “Molecular evidence for the origin of birds.” PNAS 91: 2621-2624. http://www.pnas.org/cgi/content/abstract/91/7/2621
- Hedges, S. B., and Poling, L. L. (1999) “A molecular phylogeny of reptiles.” Science 283: 998-1001. PubMed
- Hendy, M. D., Little, C. H. C., and Penny, D. (1984) “Comparing trees with pendant vertices labelled.” SIAM J. Appl. Math. 44: 1054-1065.
- Hillis, D. M. (1991) “Discriminating between phylogenetic signal and random noise in DNA sequences.” In Phylogenetic analysis of DNA sequences. pp. 278-294 M. M. Miyamoto and J. Cracraft, eds. New York: Oxford University Press.
- Hillis, D. M., and Bull, J. J. (1993) “An empirical test of bootstrapping as a method for assessing confidence on phylogenetic analysis.” Syst. Biol. 42: 182-192.
- Hillis, D. M., and Huelsenbeck, J. P. (1992) “Signal, noise, and reliability in molecular phylogenetic analyses.” Journal of Heredity 83: 189-195. PubMed
- Hillis, D. M., Moritz, C. and Mable, B. K. Eds. (1996) Molecular systematics. Sunderland, MA: Sinauer Associates.
- Hinegardner, T. T., and Engelberg, J. (1963) “Rationale for a Universal Genetic Code.” Science 142: 1083-1085.
- Hitchin, R., and Benton, M. J. (1997) “Congruence between parsimony and stratigraphy: comparisons of three indices.” Paleobiology 23: 20-32.
- Hofreiter, M., Serre, D., Poinar, H. N., Kuch, M., and Paabo, S. (2001) “Ancient DNA.” Nat Rev Genet 2: 353-359.
- Holmes, E. C., Zhang, L. Q., Simmonds, P., Rogers, A. S. and Brown, A. J. (1993) “Molecular investigation of human immunodeficiency virus (HIV) infection in a patient of an HIV-infected surgeon.” J Infect Dis 167: 1411-4. PubMed
- Hudson, R. R. (1992) “Gene trees, species trees and the segregation of ancestral alleles.” Genetics 131: 509-513. PubMed
- Huelsenbeck, J. P. (1994) “Comparing the stratigraphic record to estimates of phylogeny.” Palaeobiology 20: 470-483.
- Huelsenbeck, J. P., Ronquist, F., Nielsen, R., and Bollback, J. P. (2001) “Bayesian inference of phylogeny and its impact on evolutionary biology.” Science 294: 2310-2314. PubMed
- Ji, Q., Norell, M. A., Gao, K-Q., Ji, S-A., and Ren, D. (2001) “The distribution of integumentary structures in a feathered dinosaur.” Nature 410: 1084-1088. PubMed
- Judson, H. F. (1996) The Eighth Day of Creation: Makers of the Revolution in Biology. Expanded edition. Cold Spring Harbor Press.
- Kardong, K. V. (2002) Vertebrates: Comparative Anatomy, Function, Evolution. Third ed. New York: McGraw Hill.
- Klassen, G. J., Mooi, R. D., and Locke, A. (1991) “Consistency indices and random data.” Syst. Zool. 40:446-457.
- Kemp, J. S. (1982) Mammal-like reptiles and the origin of mammals. New York: Academic Press.
- Kestenbaum, D. (1998) “Gravity Measurements Close in on Big G.” Science 282: 2180-2181. http://www.sciencemag.org/cgi/content/full/282/5397/2180
- Krings, M., Capelli, C., Tschentscher, F., Geisert, H., Meyer, S., von Haeseler, A., Grossschmidt, K., Possnert, G., Paunovic, M., and Paabo, S. (2000) “A view of Neandertal genetic diversity.” Nat Genet 26: 144-146.
- Lehman, N. (2001) “Please release me, genetic code.” Current Biology 11: R63-R66. PubMed
- Li, W.-H. (1997) Molecular Evolution. Sunderland, MA: Sinauer Associates.
- Luo, Z.-X., Crompton, A. W. and Sun, A.-L. (2001) “A new mammaliaform from the early Jurassic and evolution of mammalian characteristics.” Science 292: 1535-1539. PubMed
- Lyons-Weiler, J., Hoeker, G. A., and Tausch, R. J. (1996) “Relative Apparent Synapomorphy Analysis (RASA) I: The Statistical Measurement of Phylogenetic Signal.” Mol. Biol. Evol. 13: 749-757. http://www. molbiolevol.org/cgi/content/abstract/13/6/749
- Machuca, R., Jorgensen, L. B., Theilade, P. and Nielsen, C. (2001) “Molecular investigation of transmission of human immunodeficiency virus type 1 in a criminal case.” Clin Diagn Lab Immunol 8: 884-90. PubMed
- Maddison, W. P., and Maddison, D. R. (1992) MacClade. Sunderland, MA: Sinauer Associates.
- Maley, L. E., and Marshall, C. R. (1998) “The coming age of molecular systematics.” Science 279: 505-506. PubMed
- McLaughlin, P. J., and Dayhoff, M. O. (1973) “Eukaryote evolution: a view based on cytochrome c sequence data.” Journal of Molecular Evolution 2: 99-116.
- Nichols, R. (2001) “Gene trees and species trees are not the same.” Trends Ecol Evol. 16: 358-364. PubMed
- Norell, M. A., and Clarke, J. A. (2001) “Fossil that fills a critical gap in avian evolution.” Nature 409: 181-184. PubMed
- Norell, M. A., Ji, Q., Gao, K., Yuan, C., Zhao, Y., and Wang, L. (2002) ”'Modern' feathers on a non-avian dinosaur.” Nature 416: 36-37. PubMed
- Norell, M. A. and Novacek, M. J. (1992a) “Congruence between superpositional and phylogenetic patterns: Comparing cladistic patterns with fossil records.” Cladistics 8: 319-337.
- Norell, M. A. and Novacek, M. J. (1992b) “The fossil record and evolution: Comparing cladistic and paleontologic evidence for vertebrate history.” Science 255: 1690-93.
- Norris, J. R. (1997) Markov Chains. Cambridge: Cambridge University Press.
- Osborn, H. F. (1918) The Origin and Evolution of Life. New York: Charles Scribner's Sons.
- Ou, C. Y., Ciesielski, C. A., Myers, G., Bandea, C. I., Luo, C. C., Korber, B. T., Mullins, J. I., Schochetman, G., Berkelman, R. L., Economou, A. N. and et al. (1992) “Molecular epidemiology of HIV transmission in a dental practice.” Science 256: 1165-71. PubMed
- Patterson, C., Williams, D., and Humphries, C. (1993) “Congruence between molecular and morphological phylogenies.” Annual Review of Ecology and Systematics 24: 153-188.
- Pei, M. (1949) The Story of Language. Philadelphia: Lippincott.
- Penny, D., and Hendy, M. D. (1986) “Estimating the reliability of phylogenetic trees.” Mol. Biol. Evol. 3: 403-417. http://www. molbiolevol.org/cgi/content/abstract/3/5/403
- Penny, D., Foulds, L. R., and Hendy, M. D. (1982) “Testing the theory of evolution by comparing phylogenetic trees constructed from five different protein sequences.” Nature 297: 197-200.
- Penny, D., Hendy, M. D., and Steel, M. A. (1991) “Testing the theory of descent.” In Phylogenetic Analysis of DNA Sequences, eds. Miyamoto, M. and Cracraft, J., New York: Oxford University Press. pp. 155-183.
- Qiang, J., Currie, P. J. et al. (1998) “Two feathered dinosaurs from northeastern China.” Nature 393: 753-761.
- Quinn, T. (2000) “Measuring big G.” Nature 408: 919-921.
- Rasoloarison, R. M., Goodman, S. M., and Ganzhorn, J. U. (2000) “Taxonomic revision of mouse lemurs (Microcebus) in the western portions of Madagascar.” International Journal of Primatology. 21(6): 963-1019.
- Ringe, D. (1999) “Language classification: scientific and unscientific methods.” in The Human Inheritance, ed. B. Sykes. Oxford: Oxford University Press, pp. 45-74.
- Rozenski, J., Crain, P. F. et al. (1999) “The RNA Modification Database: 1999 update.” Nucleic Acids Research 27: 196-197. http://medlib.med.utah.edu/RNAmods/
- Sereno, P. C. (1999) “The Evolution of Dinosaurs.” Science 284: 2137-2147. PubMed
- Stanley, S. (1993) Earth and Life Through Time. New York: W. H. Freeman.
- Steel, M. A., and Penny,D. (1993) “Distributions of tree comparison metrics—some new results.” Systematic Biology 42: 126-141.
- Strait, D. S., Grine, F. E., and Moniz, M. A. (1997) “A reappraisal of early hominid phylogeny.” J Hum Evol 32: 17-82.
- Swofford, D. L., Olsen, G. J., Waddell, P. J., and Hillis, D. M. (1996) “Phylogenetic inference.” In Molecular Systematics, pp 407-514. Hillis, D. M., Moritiz, C. and Mable, B. K. eds., Sunderland, Massachusetts: Sinauer.
- Thalmann, . U., and Geissmann, T. (2000) “Distribution and geographic variation in the western woolly lemur (Avahi occidentalis) with description of a new species (A. unicolor).” International Journal of Primatology. 21(6): 915-941.
- Thewissen, J. G, Williams, E. M., Roe, L. J., and Hussain, S. T. (2001) “Skeletons of terrestrial cetaceans and the relationship of whales to artiodactyls.” Nature. 413: 277-281. PubMed
- van Roosmalen, M. G. M., van Roosmalen, T., Mittermeier, R. A., and Rylands, A. B. (2000) “Two new species of marmoset, genus Callithrix Erxleben, 1777 (Callitrichidae, Primates), from the Tapajos/Madeira interfluvium, south central Amazonia.” Neotropical Primates 8(1): 2-18.
- Veenstra, J., Schuurman, R., Cornelissen, M., van't Wout, A. B., Boucher, C. A., Schuitemaker, H., Goudsmit, J. and Coutinho, R. A. (1995) “Transmission of zidovudine-resistant human immunodeficiency virus type 1 variants following deliberate injection of blood from a patient with AIDS: characteristics and natural history of the virus.” Clin Infect Dis 21: 556-60. PubMed
- Voet, D., and Voet, J. (1995) Biochemistry. New York: John Wiley and Sons.
- Vogel, G. (1997) “Phylogenetic analysis: getting its day in court.” Science 275: 1559-60. PubMed
- Wadsworth, H. M. (1997) Handbook of statistical methods for engineers and scientists. New York: McGraw-Hill Pub. Co.
- Wang, Y. Hu, Y., Meng, J. and Li,C. (2001) “An ossified meckel's cartilage in two Cretaceous mammals and origin of the mammalian middle ear.” Science 294: 357-361. PubMed
- Wills, M. A. (1999) “Congruence between phylogeny and stratigraphy: Randomization tests and the gap excess ratio.” Syst. Biol. 48: 559-580.
- Wilson, E. O. (1992) The Diversity of Life. Cambridge, MA, Harvard University Press.
- Wise, K. P. (1994) “The Origin of Life's Major Groups.” In The Creation Hypothesis, pp. 211-234. Moreland, J. P. ed., Downers Grove, IL: InterVarsity Press.
- Woese, C. (1998) “The universal ancestor.” PNAS 95: 6854-6859. http://www.pnas.org/cgi/ content/full/95/12/6854
- Wu, C. I. (1991) “Inferences of species phylogeny in relation to segregation of ancient polymorphisms.” Genetics 127: 429-435. PubMed
- Xu, X., Tang, Z-T., Wang, X-l. (1999) “A therizinosauroid dinosaur with integumentary structures from China.” Nature 399: 350-354.
- Xu, X., Zhou, Z., and Wang ,X. (2000) “The smallest known non-avian theropod dinosaur.” Nature 408: 705-708 PubMed
- Xu, X., Norell, M. A., Wang, X-l., Makovicky, P. J., and Wu, X.C. (2002) “A basal troodontid from the Early Cretaceous of China.” Nature 415: 780-784. PubMed
- Yirrell, D. L., Robertson, P., Goldberg, D. J., McMenamin, J., Cameron, S. and Leigh Brown, A. J. (1997) “Molecular investigation into outbreak of HIV in a Scottish prison.” Bmj 314: 1446-50. http://bmj.com/cgi/content/full/314/7092/1446?view=full&pmid=9167560
- Yockey, H. P. (1992) Information Theory and Molecular Biology. New York: Cambridge University Press.
- Yoder, A. D., Rasoloarison, R. M., Goodman, S. M., Irwin, J. A., Atsalis, S., Ravosa, M. J., and Ganzhorn, J. U. (2000) “Remarkable species diversity in Malagasy mouse lemurs (primates, Microcebus).” Proc Natl Acad Sci 97(21): 11325-30. http://www.pnas.org/cgi/ content/full/97/21/11325
- Zhu, T., B. Korber, et al. (1998) “An African HIV-1 sequence from 1959 and implications for the origin of the epidemic.” Nature 391: 594-597. PubMed
- Zuckerkandl, E. and Pauling, L. (1965) “Evolutionary Divergence and Convergence in Proteins.” in Evolving Genes and Proteins: a symposium held at the Institute of Microbiology of Rutgers, with support from the National Science Foundation. Eds Vernon Bryson and Henry J. Vogel. New York: Academic Press.